| Dictionnaire médical |
Abréviations P Pach Paid Pala Palato Pali Palu Palud Pamp Pan Panc Pancréat Pans Papi Papill Par Para Pare Pari Paro Parv Paré Pate Patell Path Pauc Paus Pedi Pell Pelv Peps Pept Per Pert Pest Peti Pexi Phac Phaco Phag Phak Phal Phaq Phar Pharmaco Pharyngo Phas Phil Phim Phle Phlegmo Phlé Phlébo Phob Phor Phos Phosphato Phot Photo Phré Phréno Phti Phys Physio Phyt Phyto Phén Phéno Phéo Pian Pied Pigm Pila Pile Pili Pilo Pituito Pity Pityro Plac Placento Plas Plasmo Plat Platino Platy Pleu Pleuro Plur Plèv Pléi Pléio Pléo Plét Pneu Pneumo Pod Podo Poecilo Poikilo Poil Poli Polio Poll Pollaki Poly Pomm Pomp Ponc Pore Pori Poro Porp Porphyri Poso Post Pota Potasse Poto Pour Poïk Prem Pres Presby Pression Prim Primi Primo Pro Proc Proct Prod Produit Prof Prog Prom Pron Prop Pros Prostat Prot Protéin Prov Prox Proé Prur Prurig Prurit Pré Préc Prép Pseu Pseud Psit Pso Psoa Psor Psoï Psyc Psycho Pter Ptér Ptôs Ptôse Pub Pube Pubi Pubè Pulp Purp Purpura Pycn Pycno Pygo Pylo Pyo Pyod Pyog Pyoh Pyop Pyos Pyr Pyri Pyro Pyru Pyré Pyél Pyélo Pyém Pci Péd Péda Pédi Pédo Péli Pére Péri pH
| pH | |
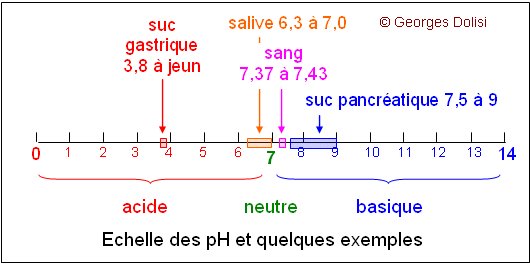
| Biochimie Abrév. Potentiel Hydrogène. La lettre H représente l'atome d'hydrogène. En effet, le pH est la mesure de l'acidité ou de l'alcalinité (ou basicité) d'une solution. Ce potentiel hydrogène est obtenu par le logarithme décimal (log) de l'inverse de la concentration en ions H+ d'une solution. Ces ions H+ proviennent de la dissociation de l'eau selon la formule H2O <--> H+ + OH- (réaction réversible). Il y a donc toujours autant d'ions H+ que d'ions OH-. On a montré expérimentalement que le produit des ions H+ et OH- reste toujours égal à 10-14 et que, dans une eau neutre à 15°C, [H+] = [OH-] = 10-7. Un composé est dit acide quand il libère, par dissociation, plus d'ions H+ que d'ions OH- ; il est basique (ou alcalin) quand il libère plus d'ions OH- que d'ions H+. L'échelle des pH va donc de 0 à 14, avec la valeur zéro pour une solution normale d'acide ayant une concentration unitaire d'un équivalent-gramme par litre et entièrement dissociée en ions hydrogène. De même la valeur 14 pour une solution normale d'alcali fort. La pH-métrie est le fait de mesurer le pH d'une solution. Exemple : dans les RGO (ou reflux gastro-sophagiens), on mesure le pH de l'sophage. Le RGO est confirmé par un pH acide.
© Georges Dolisi | |
| < vers le menu principal | Politique de confidentialité | App Privacy Policy | Contact | ^ haut de la page |
| © 2006, 2020 Medicopedia | Powered by JIMaroc |