| Dictionnaire médical |
Abréviations B Baci Bacill Bact Bactér Balan Baro Bart Basa Base Basi Baso Bath Bec Benz Bi Bibl Bica Bice Bici Bicu Bila Bilan Bile Bilh Bili Binu Bio Bioc Biod Biof Biol Biom Biot Bipo Blas Blast Blen Blenn Bleu Bloc Blépha Bobb Borb Borr Botu Bouc Bouf Bour Brac Brachi Brachy Brad Brady Brom Bron Bronch Brux Bryc Bucc Bulb Bull Burs Buty Butyr Béni Bézo Bêta
| Bicarbonates standards | |
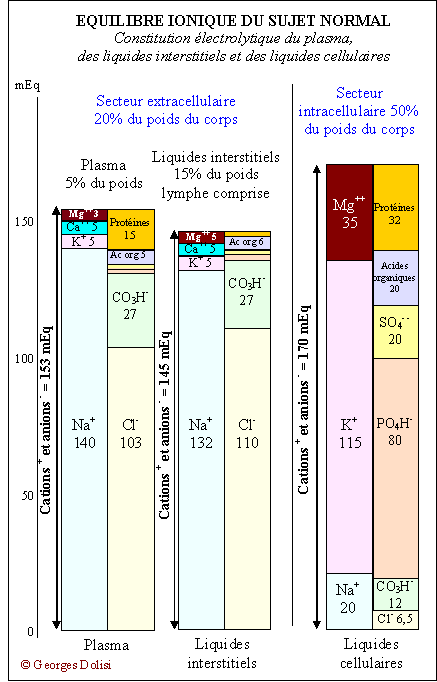
| Médecine biologique N. m. * bi : du latin bis {bi-, bis-}, deux fois, qui indique la répétition ou la duplication ; * carbo : du latin carbo, -onis {carb(o)-, charbon}, en rapport avec le carbone, corps combustible noir que lon extrait des combustibles fossiles ; * ate : du suffixe -ate qui, en chimie désigne un sel. Un bicarbonate est un sel de l'acide carbonique H2CO3, dans lequel un seul atome d'hydrogène a été remplacé par un métal.L'ion bicarbonate HCO3- est l'un des principaux anions du milieu intérieur et constitue l'essentiel de la réserve alcaline. Bicarbonates standard : c'est la concentration sanguine en ion bicarbonate. Ils jouent un rôle particulièrement important dans l'équilibre acido-basique du sang, vital pour tous les phénomènes qui se produisent dans l'organisme. Ils participent à un "système tampon" (parmi d'autres) qui peut produire en cas de besoin ou éliminer en cas d'excès des acides et des bases. Les 27 mEq de CO2 (voir ci-dessus le tableau des électrolytes) sont engagés sous forme de bicarbonate de sodium et constituent la réserve alcaline ou bicarbonates standard ou tampon bicarbonates - acide carbonique. Dans le plasma, il existe un rapport normal entre les bicarbonates et l'acide carbonique libre qui est : NaHCO3 / H2CO3 = 20 / 1. De ce rapport dépend directement le pH du sang. Comment fonctionne ce tampon ? Si dans le sang arrive un acide plus fort que l'acide carbonique (donc de pH inférieur), il est libéré de sa forme combinée en ion bicarbonate : HCO3Na → Na+ + HCO3-. L'acide carbonique étant un acide faible, il agit relativement peu sur le pH, mais il en résulte quand même une tendance à l'acidose par diminution des bicarbonates. Pour les raisons inverses, si les bicarbonates augmentent (alimentation, médicaments ...), il en résulte une tendance à l'alcalose. Les acidoses ou alcaloses qui résultent des variations du numérateur du rapport ci-dessus sont qualifiées de fixes ou métaboliques, alors que celles qui résultent des variations du dénominateur (donc de l'acide carbonique libre) sont des acidoses ou alcaloses gazeuses ou respiratoires. Dans notre corps, l'estomac produit une énorme quantité d'acide, ce qui fait que l'organisme doit lutter en permanence contre une acidose. C'est le rein qui participe le plus à cette lutte en produisant de l'ammoniaque, une base forte. * Bicarbonate de potassium : de formule KHCO3, le bicarbonate de potassium est surtout connu pour ses propriétés d'antiacide gastrique. Il entre comme excipient dans un certain nombre de médicaments, mais on le trouve aussi en pastilles effervescentes utilisées dans les carences en potassium, élément minéral indispensable au métabolisme. En nologie, il est aussi utilisé pour diminuer l'acidité des moûts.
© Georges Dolisi | |
| < vers le menu principal | Politique de confidentialité | App Privacy Policy | Contact | ^ haut de la page |
| © 2006, 2020 Medicopedia | Powered by JIMaroc |